|
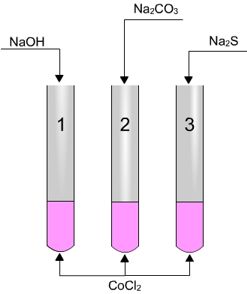
Rotular tres tubos como 1, 2 y 3. Poner
en cada uno de ellos un poco de CoCl2.
A continuación añadir:
| Tubo1:
NaOH |
| Tubo2:
Na2CO3 |
| Tubo 3:
Na2S |
| Es conveniente realizar las
reacciones consecutivamente tratando de identificar los
compuestos formados y, después, escribir y ajustar la
ecuación correspondiente. Podemos
verificar que en el tubo 1 el precipitado es Co(OH)2
observando como se transforma con el tiempo en Co(OH)3
color marrón oscuro |
|
 |
El carbonato de cobalto(II) formado en el tubo 2 se
puede identificar porque al añadir HCl (lentamente, con cuidado) se
observa la formación de burbujas de CO2 y el precipitado
se disuelve.
El sulfuro de cobalto(II) que se forma en el tubo 3
es inconfundible por su color negro intenso. No obstante, puede
confirmarse su formación añadiendo HCl. El precipitado se disolverá
formando CoCl2 que dará un aspecto rosado a la disolución
y se formará H2S (gas) fácilmente identificable por su
olor característico |