|
De una célula a otra, de una generación a la siguiente.
La
información genética que determina cómo se forman los
seres humanos se ha transmitido en nuestros cuerpos
durante cientos de miles de años y, aunque está
constantemente sometida a agresiones del medio ambiente,
permanece sorprendentemente intacta. Tomas Lindahl,
Paul Modrich y Aziz Sancar reciben el Premio Nobel de
Química 2015 por haber descrito y explicado cómo las
células reparan el ADN salvaguardando la información
genética. |
|
Nuestro ADN se
mantiene sorprendentemente intacto, año tras año, debido a
una serie de mecanismos de reparación molecular: un
enjambre de proteínas que controlan los genes. Ellas
continuamente leen el genoma y reparan cualquier daño que
se ha producido. El Premio Nobel de Química 2015 ha sido
adjudicado a Tomas Lindahl, Paul Modrich y Aziz
Sancar por haber descrito estos procesos
fundamentales a nivel molecular. Su trabajo ha significado
una contribución decisiva para la comprensión de cómo
funcionan las células, además de proporcionar conocimiento
sobre las causas moleculares de varias enfermedades
hereditarias y sobre los mecanismos de desarrollo del
cáncer y el envejecimiento.
|
"¿Cuánto de
estable es el ADN, realmente?", Tomas Lindahl
comenzó haciéndose esta pregunta a finales de la
década de 1960. Entonces la comunidad científica
consideraba que la molécula de ADN – la base de la vida –
era extremadamente resistente. La evolución requiere
mutaciones, pero solo de un número limitado por
generación. Si la información genética fuera demasiado
inestable los organismos multicelulares no podrían
existir.
Deberían de
pasar unos cuantos años antes de que comenzara a buscar
una respuesta a esa pregunta. En aquel tiempo se encontraba
en Suecia, en el Karolinska Institutet, en Estocolmo,
donde algunos experimentos le mostraron que sus sospechas eran
correctas: el ADN experimentaba una degradación lenta pero
notable. Lindahl estimó que se producían miles de lesiones
potencialmente devastadoras en el genoma cada día, una
frecuencia claramente incompatible con la vida humana. Su
conclusión fue que deberían existir sistemas moleculares
para la reparación de todos estos defectos y, con esta
idea, abrió la puerta a un nuevo campo de
investigación.
Durante
35 años Tomas Lindahl ha encontrado y examinado muchas de
las proteínas que las células emplean para la reparación
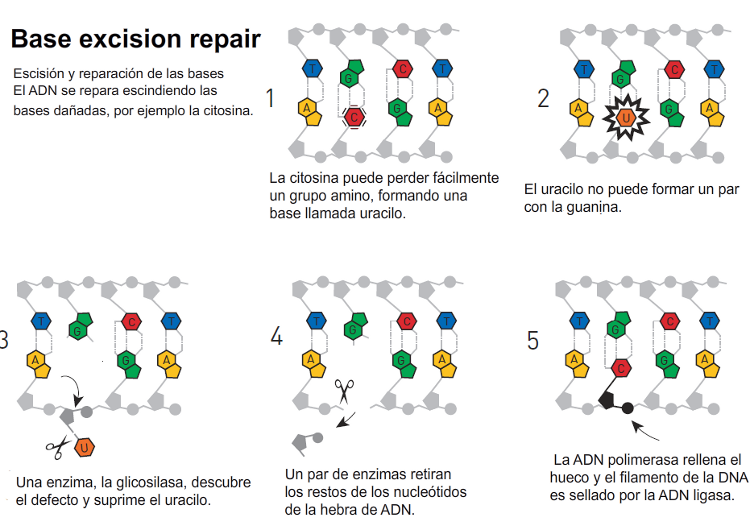
del ADN. Poco a poco, elabora una imagen molecular
de cómo se produce la supresión y reparación de las bases
dañadas, un proceso en el cual las glicosilasas,
son el primer paso en el proceso de reparación del ADN. La
escisión y reparación de las bases también se produce en
los seres humanos y, en 1996, logró recrear,
in vitro, el proceso de reparación en humanos. |
|
 |
|
|
El hecho de
que el ADN puede ser dañado por agresiones ambientales,
tales como los rayos UV, era conocido desde hacía tiempo.
El mecanismo utilizado por la mayoría de las células para
reparar el daño producidos por los rayos UV, (nucleotide
excision repair) había sido descrito por Aziz
Sancar, nacido en Savur, Turquía y que desarrolló
su carrera profesional en Estados Unidos.
En 1976,
utilizando las herramientas que la biología molecular
ponía entonces a su disposición, clonó con éxito el gen de
la enzima que repara el ADN dañado por la radiación
ultravioleta, la fotoliasa, y también bacterias
productoras de la enzima. Este trabajo se convirtió en una
tesis doctoral, pero no tuvo excesivo eco en la comunidad
científica.
Estaba claro
que las bacterias tienen dos sistemas para la reparación
del daño causado por los rayos UV: además de la fotoliasa,
que actuaba en presencia de la luz, se había descubierto
un segundo sistema que funcionaba en la oscuridad.
Tal y como
había hecho en sus anteriores estudios con la fotoliasa,
Sancar comenzó a investigar el proceso molecular en
ausencia de luz. Al cabo de algunos años había conseguido
identificar, aislar y caracterizar las enzimas codificadas
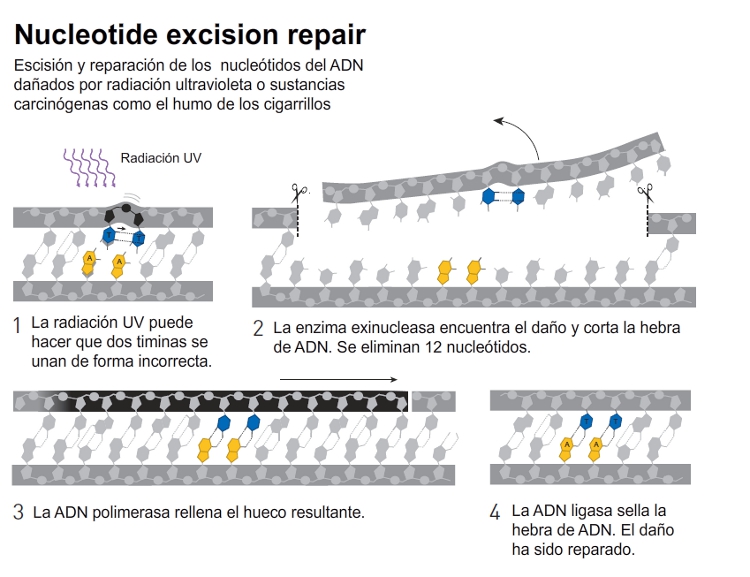
por los genes uvrA, uvrB y uvrC. En experimentos in vitro
mostró que estas enzimas pueden identificar los daños
producido por la luz UV, luego hacen dos incisiones en el
filamento del ADN, una a cada lado de la parte dañada,
y posteriormente retiran un fragmento de 12 -13
nucleótidos que incluye la parte dañada. |
|
La maquinaria
molecular que repara el daño UV en el ADN humano es más
compleja que la que actúa en las bacterias, pero, en
términos químicos, el mecanismo de reparación funciona del
mismo modo en todos los organismos. |
|
 |
|
Paul
Modrich creció en un pequeño pueblo en el norte de
nuevo México, Estados Unidos. Un día su padre, profesor de
biología, le comentó: "Deberías aprender cosas sobre el
ADN". Esto fue en 1963. Unos años más tarde, esas "cosas
del ADN" llegaron a ser centrales en la vida de Paul
Modrich. Desde el comienzo de su carrera como
investigador, como estudiante de doctorado en Stanford,
durante su postdoctorado en Harvard y como profesor
asistente en la Universidad de Duke, examinó una serie de
enzimas relacionadas con el ADN: la ADN ligasa, la
ADN polimerasa y la enzima Eco RI. Cuando
posteriormente, a finales de la década de 1970, centró su
atención a la enzima Dam metilasa se encontró con
otra "cosa de ADN" que ocuparía gran parte de su carrera
como científico.
La Dam
metilasa une grupos metilo al ADN. Paul Modrich demostró
que estos grupos metilo podrían funcionar como postes
indicadores, ayudando a la enzima a cortar la cadena de
ADN en el lugar correcto.
En este punto
los caminos de Paul Modrich y de Matthew Meselson,
un biólogo molecular de la Universidad de Harvard, se
cruzaron. Trabajando juntos crearon un virus con una serie
de desajustes en su ADN. Esta vez la dam metilasa de
Modrich fue utilizada para agregar grupos metilo a una de
las hebras de ADN. Cuando estos virus infectaban
bacterias, las bacterias corregían el filamento de ADN que
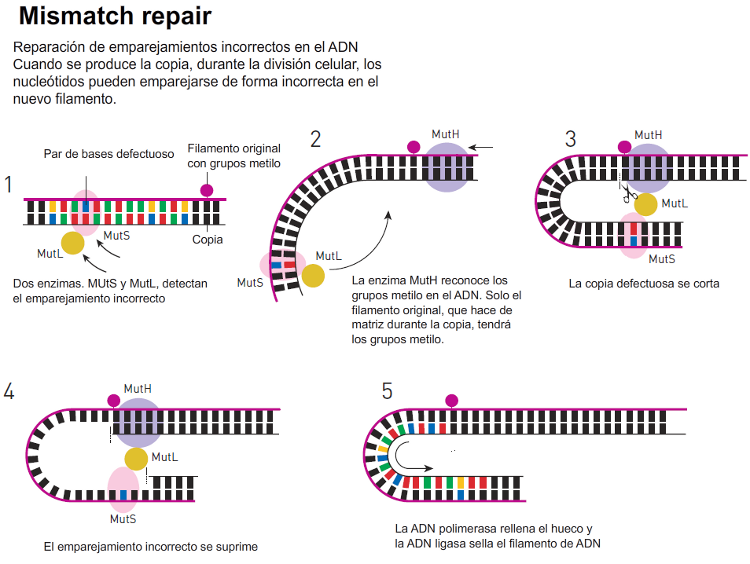
carecía de grupos metilo. La conclusión de Modrich y de
Meselson fue que la reparación del ADN es un proceso
natural que corrige los fallos que se producen cuando se
copia el ADN, reconociendo el filamento defectuoso por no
estar metilado.
Para Paul
Modrich este descubrimiento inició una década de trabajo
sistemático, clonando y estudiando las enzimas que toman
parte en el proceso de reparación. Hacia el final de la
década de 1980, fue capaz de recrear el mecanismo de
reparación molecular in vitro y estudiarlo con
gran detalle. Este trabajo fue publicado en 1989. |
|
 |
|
Además de la
reparación de las bases, y la reparación de desajustes de
la cadena, hay varios mecanismos que mantienen nuestro
ADN. Cada día tienen lugar miles de daños en el ADN,
causados por el sol, el humo de los cigarrillos u otras
sustancias genotóxicas; continuamente, en cada división
celular, miles de alteraciones del ADN son corregidas. Nuestro genoma se derrumbaría sin estos
mecanismos de reparación. Si un componente falla, la
información genética cambia rápidamente y aumenta el
riesgo de cáncer.
Daños
congénitos en el proceso de escisión y reparación de los
nucleótidos son la causa de la enfermedad conocida con el
nombre de xeroderma pigmentosa. Los individuos que la
padecen son extremadamente sensibles a la radiación UV y
desarrollan cáncer de piel si se exponen al sol. Defectos
en la reparación del ADN aumentan el riesgo de desarrollar
cáncer de colon hereditario, por ejemplo.
De hecho, en
muchas formas de cáncer, uno o más de estos sistemas de
reparación han sido parcial o totalmente desactivados.
Esto hace que el ADN de las células cancerosas sea
inestable, de ahí que las células cancerosas a menudo
mutan y se vuelven resistentes a la quimioterapia. Al
mismo tiempo, estas células enfermas son muy dependientes
de los sistemas de reparación que siguen funcionando; sin
éstos su ADN podría dañarse seriamente provocando la
muerte de las células. Los investigadores están intentando
aprovechar todo esto para el desarrollo de nuevos fármacos
contra el cáncer. Inhibiendo un sistema de reparación
pueden frenar o detener completamente el crecimiento del
cáncer. Un ejemplo de un fármaco que inhibe un sistema de
reparación de las células cancerosas es el Olaparib.
En conclusión,
la investigación básica realizada por los laureados con el
Premio Nobel de Química de este año no solo ha aumentado
nuestro conocimiento sobre procesos moleculares básicos,
también sus investigaciones podrían conducir al desarrollo
de tratamientos que salven vidas.
|
|