|
|
|
Hasta
finales de los setenta, el interés por las proteínas se
había centrado en estudiar su síntesis, pero poco esfuerzo
se había realizado para entender el proceso opuesto, el cómo
y el por qué las proteínas se degradaban.
El
Premio Nóbel de este año es compartido por tres científicos
que han realizado importantes descubrimientos para entender
cómo las células regulan la degradación de las proteínas.
|

Aaron
Ciechanover
|

Avran
Hershko
|

Irwin
Rose.
|
"Por
el descubrimiento de la función de la ubiquitina como
mediadora en la degradación de las proteínas."
|
|
Aaron
Ciechanover (1947). Israel
Avran
Hershko (1937). Israel
Irwin
Rose. (1926). U.S.A. |
|
|
Aaron
Ciechanover, Avran Hershko e Irwin Rose, descubrieron la proteolisis (ruptura
de las proteínas) mediada por la ubiquitina.
La
degradación de una proteína mediante este proceso tiene lugar en dos etapas:
-
Proceso
de "marcado" de la proteína a degradar.
-
Degradación
de la proteína marcada, dando lugar a sus componentes (aminoácidos).
Los
premiados de este año lo han sido por dilucidar el mecanismo mediante el cual
se produce el "marcado" de las proteínas.
Según
sus trabajos (realizados a principio de los ochenta), el marcaje se lleva a
cabo mediante una pequeña proteína (de tan solo 76 aminoácidos) conocida
con el nombre de ubiquitina (descubierta en 1975 por Goldstein y col).
|
|
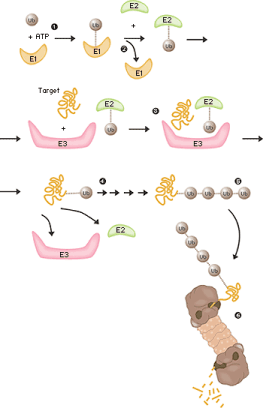
El
mecanismo mediante el cual se produce el etiquetado de la proteína que va a
ser degradada se realiza en varios pasos:
-
La
ubiquitina es transportada por una enzima (activador de ubiquitina)
conocida como E1 que la transfiere a una segunda enzima E2 (conjugador de
ubiquitina).
-
Una
trecera enzima E3 (ligasa de ubiquitina) entra en escena para
transferir la ubiquitina desde la enzima E2 hasta la "proteína
diana" que de esta manera comienza su proceso de marcado.
-
El
proceso anterior se repite varias veces hasta que la proteína diana
acumula, al menos, cuatro moléculas de ubiquitina, momento en el que ya
está lista para su degradación.
-
La
degradación es realizada por la proteosoma, una estructura en forma de
barril, que tritura la proteína liberando los aminoácidos y las
moléculas de ubiquitina que quedan disponibles para ser reutilizadas.
|
|
|
La
importancia del descubrimiento es alta ya que el procedimiento está implicado
en algunas enfermedades humanas como el cáncer, la fibrosis quística o el
mal de Alzheimer, patologías en las cuales se observa un mal funcionamiento
del mecanismo de eliminación de las proteínas. Así la proteína p53,
conocida como "el guardián del genoma" tiene por misión reparar
las moléculas de ADN eliminando mutaciones que pudieran ser peligrosas. Pues
bien, en ciertas ocasiones esta proteína
es degradada incorrectamente por la ubiquitina, provocándose la acumulación
de mutaciones que acaban provocando cáncer.
La
ubiquitina, sorprendentemente, tiene una estructura básicamente idéntica en
las levaduras y en los seres humanos. Un ejemplo más de cómo tras una
aparente diversidad la vida funciona siguiendo patrones comunes en todos los
seres vivos.
|
|
|